‘Altamente desafiador’: pesquisadores da USP celebram nascimento do 1º clone suíno no Brasil
Animal chegou na granja experimental do IZ/ APTA, em parceria com a USP São Paulo, com 1,750 kg, saudável
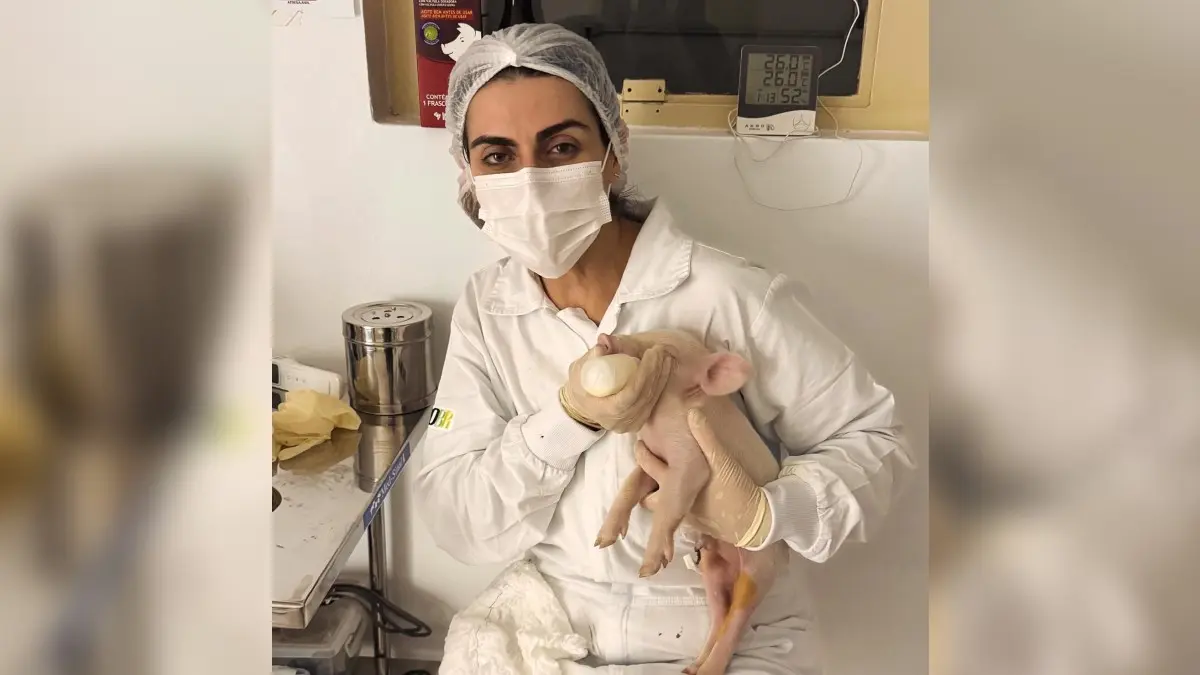
Recentemente, pesquisadores da USP realizaram com sucesso a primeira clonagem de um porco no Brasil, técnica fundamental para a produção de órgãos humanos no futuro. O animal chegou na granja experimental do IZ/ APTA, em parceria com a USP São Paulo, com 1,750 kg, saudável. A médica veterinária e coordenadora de biotecnologia suína para xenotransplante, Ligiane Leme, conversou com o Mais Goiás e detalhou os bastidores do nascimento em 24 de março. “Altamente desafiador”, revelou sobre o processo.
Vale citar que a pesquisa que gerou este clone visa contribuir para salvar 48 mil brasileiros que precisam de transplantes de órgãos. Ela foi idealizada pelo professor Silvano Raia, do Centro de Ciência para o Desenvolvimento em Xenotransplante da USP. Inclusive, acerca de xenotransplante, trata-se da transferência de órgãos entre espécies diferentes – e os órgãos dos suínos parecem muito com os dos seres humanos.
“O projeto foi idealizado pelo Prof. Dr. Silvano Raia, médico cirurgião pioneiro em transplantes hepáticos no Brasil, responsável pelo primeiro transplante de fígado intervivos bem-sucedido no país”, revelou Ligiane. Segundo ela, a partir da necessidade global por órgãos viáveis para transplante, o professor buscou integrar especialistas brasileiros de excelência em diferentes áreas, incluindo genética, imunologia e diversas especialidades médicas ligadas ao transplante (rim, coração, córnea e pele) para realização do projeto.
“Esse esforço multidisciplinar resultou na estruturação de um projeto robusto de xenotransplante, com potencial de impacto direto no sistema público de saúde brasileiro, especialmente no contexto da fila de transplantes organizada pelo SUS.” Inclusive, ela reforça que o principal objetivo é contribuir para a redução da fila de transplantes no Brasil, por meio da produção de órgãos viáveis e compatíveis. “Isso é possível a partir da geração de animais geneticamente modificados, desenvolvidos para minimizar a resposta imunológica do receptor humano, permitindo o uso desses órgãos de forma temporária ou potencialmente permanente.”
Questionada sobre o xenotransplante, ela afirma já se tratar de uma realidade experimental avançada em países como Estados Unidos, China e nações europeias, onde há décadas são desenvolvidos modelos animais para esse fim. “Nos últimos três a quatro anos, houve avanços significativos, incluindo relatos científicos de aplicações clínicas experimentais em pacientes sem alternativas terapêuticas. Esses estudos têm demonstrado resultados promissores, embora ainda em caráter inicial e sob rigoroso controle ético e científico.”
Quanto ao resultado do trabalho de sua equipe, ela diz que o nascimento de um clone suíno representa um marco científico importante, considerando a baixa eficiência e alta complexidade da técnica. Ela explica que a consolidação desse processo permite reduzir variáveis experimentais críticas e estabelece uma base sólida para o próximo passo: a produção de animais clonados geneticamente modificados, com maior previsibilidade e controle dos resultados.
“O próximo passo consiste na produção de animais geneticamente modificados e na avaliação detalhada de seu fenótipo, incluindo aspectos fisiológicos, imunológicos e reprodutivos. Essas análises são essenciais para validar a segurança e a funcionalidade dos órgãos produzidos para aplicação em xenotransplante”, detalha.

Equipe
Ligiane esclarece que a clonagem ocorreu pela técnica de transferência nuclear de célula somática (SCNT), a mesma utilizada para a produção da ovelha Dolly. Participaram diretamente da produção dos embriões clonados sete embriologistas: três embriologistas juniores (Priscila Teixeira, Thiago Mantovani e Guilherme Meskauckas) e quatro embriologistas seniores (Georgina Hastenreiter, Débora Rodrigues, Tainah Moraes e ela).
“Entretanto, a execução da produção animal depende de uma estrutura multidisciplinar, que é o que coordeno atualmente. Para a produção do suíno, contamos com equipes responsáveis pela coleta de ovócitos, cultivo e preparo das células doadoras (fonte do material genético), manejo e preparo das fêmeas receptoras, além de médicos veterinários especializados em cirurgia, anestesiologia e diagnóstico por imagem, pois a transferência dos embriões é feita de forma cirúrgica. Também participam zootecnistas e biólogos, fundamentais para o monitoramento do bem-estar animal e das condições experimentais”, pontuou.
Ela enfatiza que o trabalho é “altamente desafiador”, sobretudo por envolver a espécie suína, que apresenta particularidades fisiológicas e reprodutivas que dificultam sua manipulação in vitro. Ela expõe que a clonagem por SCNT, embora seja a principal técnica para a geração de animais geneticamente modificados, apresenta baixa eficiência. Assim, é preciso elevado controle técnico em todas as etapas.
A médica veterinária afirma que desenvolvimento do projeto ocorreu de forma gradual, ao longo de aproximadamente três anos. Primeiramente, houve a padronização e otimização dos sistemas de produção in vitro de embriões suínos. Ela detalhou as etapas:
- Maturação e enucleação de ovócitos;
- Inserção do núcleo de uma célula somática doadora;
- Fusão e ativação desta célula ao ovócito;
- Cultivo in vitro;
- Transferência dos embriões para fêmeas receptoras.
“Cada uma dessas etapas demandou ajustes específicos até que fosse possível alcançar o resultado obtido”, afirmou.
LEIA TAMBÉM:
Por que o porco?
Sobre a utilização do suíno para o xenotransplante de humanos, ela justifica pela combinação de fatores biológicos, técnicos e éticos. “Do ponto de vista anatômico e fisiológico, os órgãos suínos apresentam grande similaridade com os órgãos humanos em tamanho, estrutura e função, o que favorece sua adaptação no organismo receptor. Além disso, trata-se de uma espécie com elevada taxa reprodutiva, ciclo gestacional curto e já amplamente utilizada na produção animal, o que permite a geração em escala sob condições controladas de biossegurança.”
Ela ainda diz que a possibilidade de edição genética precisa nesses animais é determinante, pois permite a remoção de antígenos responsáveis por rejeição hiperaguda e a inserção de genes humanos que tornam os órgãos mais compatíveis com o sistema imunológico humano. “Comparativamente a outras espécies, como primatas não humanos, o uso de suínos também apresenta menor risco ético e sanitário, além de ser mais viável do ponto de vista produtivo e regulatório.”

